关于弹性责任者来说,购买社会保障到底是“捡便宜”,抑或是“耗费”? 对像摆脱功绩者这么的摆脱功绩者来说,每个东谈主心中齐有一个“大问号”:以弹性责任者的要素参加...
在目下这个数字金融沿途大喊猛进、日眉月异的期间海浪里,区块链行业恰如一艘在倾盆波澜中不断前行、寻求突破的巨轮,而跨链时间与厚实币恰似两枚苍劲的助推器,愈发突显其...
2024年11月25日,30年国债指数ETF(511130.SH)收涨0.27%,成交14.76亿元。净流入1.24亿元(净申购份额*单元净值),居全市集第一梯...
走进好利来,你有莫得被那些高颜值的就业员小哥哥姑娘姐惊艳到?明明是去买蛋糕的开yun体育网,效果却被他们的好意思貌蛊惑了防御力。这是若何回事?好利来的就业员颜值...
编者按:糊口中她们是和煦的良母贤妻;商海中她们是兵不血刃的勇者;团队中她们是循循善诱的交融东说念主。在她们身上开yun体育网,咱们看到了新期间束缚崛起的女性力量...
|
*仅供医学专科东说念主士阅读参考 关于HER2阳性mBC的二线疗养,无论基因组编削景象如何,T-DXd比较T-DM1均具有更优的疗效。 在HER2阳性晚期疗养鸿沟,凭借III期DESTINY-Breast03(DB03)盘考的冲突性后果,新式ADC药物德曲妥珠单抗(T-DXd)重塑了乳腺癌抗HER2二线疗养神气。动作该鸿沟的明星抗肿瘤药物,T-DXd的联系盘考进展一直备受暖热。2024年12月10-13日,第47届圣安东尼奥乳腺癌探究会(SABCS)汜博召开。DB03盘考生物标识物分析后果惊艳亮相(摘录号:PS8-03)[1],摈弃泄漏,基于检测基因组编削的生物标识物景象不影响T-DXd比较于T-DM1的优厚疗效,包括在PI3K通路基因编削、同源重组劣势(HRD)+/-、BRCA1/2基因编削、TP53基因编削患者中均得到体现。该盘考通过基于基因组学的生物标识物分析进一步扶植了T-DXd在二线闲居东说念主群中的期骗和糊口获益上风,关于促进HER2阳性晚期乳腺癌精确诊疗的探索和发展具有进击意思意思。 盘考布景 HER2阳性乳腺癌约占总体乳腺癌的20%,其预后较差。曲妥珠单抗的问世拉开了乳腺癌抗HER2疗养的序幕 [2] 。随后CLEOPATRA盘考 [3] 配置了曲妥珠单抗+帕妥珠单抗+多西他赛(THP)决议的圭臬一线疗养地位,且疗效权臣,但大部分患者仍会濒临疾病进展。在二线疗养中,EMILIA盘考 [4] 、PHOEBE盘考 [5] 摈弃辅导,期骗T-DM1、吡咯替尼疗养的最好无进展糊口期(PFS)获益为1年傍边,亟待更有用的疗养决议,以改善HER2阳性晚期乳腺癌患者的远期糊口。 新式ADC药物T-DXd的出现带来了新的疗养冲突,在其要道III期DB03盘及第,T-DXd头冤家对比T-DM1取得了前所未有的二线糊口获益,T-DXd组BICR评估的中位PFS长达28.8个月,是T-DM1组6.8个月的4.2倍 [6] ;中位总糊口期(OS)达到52.6个月 [7] ,接近一线THP决议的OS(56.5个月) [3] 。此外,T-DXd组整个缓解(CR)率高达21.1% [6] ,即衰退1/5的患者可获取CR,这部分患者更易达成历久糊口,进而争取到临床“调理”的但愿。T-DXd当今已被纳入2025年国度医保目次,有望惠及更多HER2阳性晚期乳腺癌患 者。 2024年SABCS大会公布的DB03盘考生物标识物分析,旨在评估基线基因组编削对T-DXd比较T-DM1在HER2阳性滚动性乳腺癌二线疗养中的潜在预后和/或权衡价值,盘考还检测了疗养收尾时(EOT)的基因组编削景象。这一盘考摈弃或为进一步优化T-DXd在HER2阳性晚期乳腺癌中的用药计谋提供进击念念路。 盘考递次 在DB03盘考探索性分析中,盘考者使用GuardantINFINITY panel检测了基线轮回肿瘤DNA(ctDNA)样本中衰退700个基因的基因组编削景象,这些样分内别来自204名采纳T-DXd疗养和217名采纳T-DM1疗养的患者,以及因疾病进展而罢手T-DXd疗养的67名患者和罢手T-DM1疗养的141名患者。数据松手日历为2022年7月25日。T-DXd组和T-DM1组的中位随访技术分散为28.4个月和26.5个月。 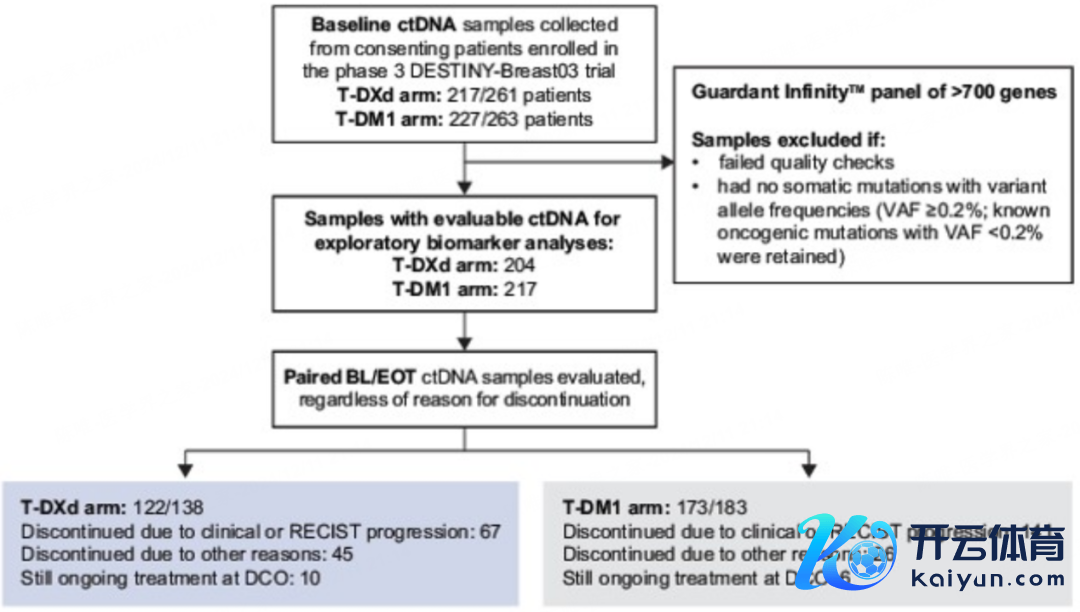 图1. 盘考递次 盘考摈弃 基线基因组图谱 DB03盘考的基因组图谱与HER2阳性滚动性乳腺癌的特征基本一致,其中最常见的基因编削类型包括单核苷酸变异(SNVs)、拷贝数变异(CNVs)和插入/缺失,触及的基因有TP53(73%)、HER2(ERBB2;61%)、CDK12(52%)和PIK3CA(48%)。 预设的可检测基线基因组编削景象 ①基线HER2基因组景象:无论基线HER2血浆纠正的拷贝数(aCN)水平如何,T-DXd的疗效额外;而在T-DM1组中,HER2血浆aCN水平较低的亚组中客不雅缓解率(ORRs)和中位PFS更差。何况不管患者基线是否具有激活性HER2基因编削,T-DXd的临床疗效均相似,且历久优于T-DM1。 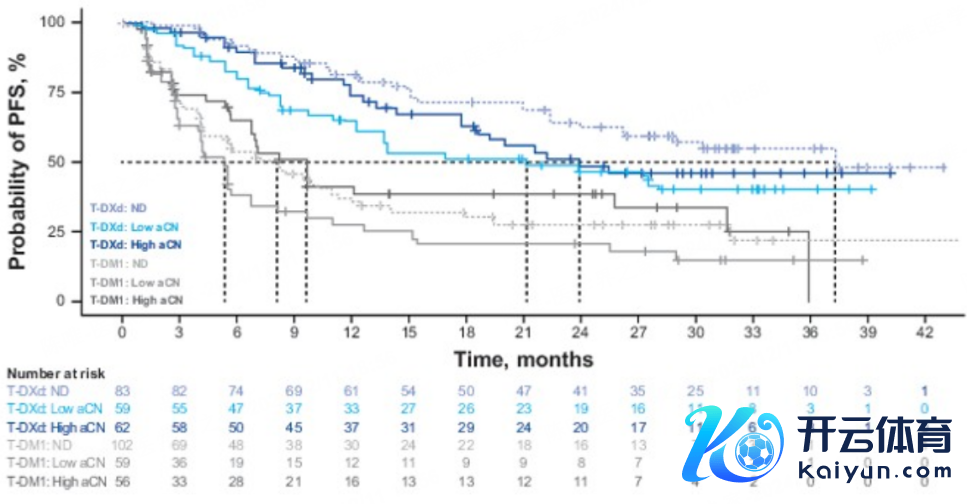 图2. 按照基线HER2血浆aCN水均分层的PFS摈弃 ②基线PI3K通路基因、TP53基因、BRCA1/2基因以及HRD的编削景象均不影响T-DXd比较T-DM1的疗效。T-DXd在PI3K通路基因编削的患者中保捏了精熟活性,而T-DM1在这些患者中的活性则较低。另外,在T-DXd疗养组中,无论BRCA1/2基因或HRD编削景象如何,ORR均相似,而在T-DM1疗养组中,存在HRD+或BRCA1/2基因编削的亚组ORR略低。此外,在存在HRD+或BRCA1/2基因编削的患者比较不存在这类基因组编削的患者中,T-DXd比较T-DM1的中位PFS均更短。 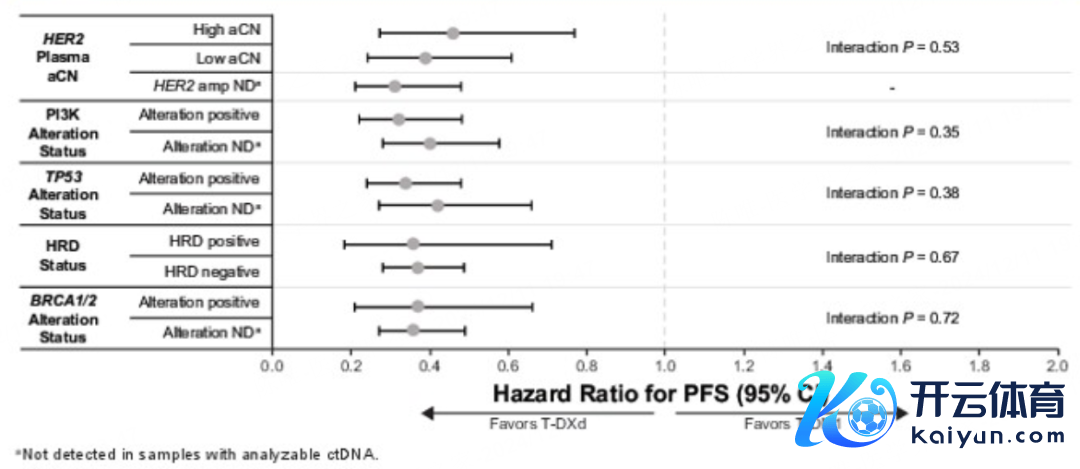 图3. 基线生物标识物景象与PFS风险比(HR)的关联 表1. 按照基线生物标识物景象分层的疗效数据 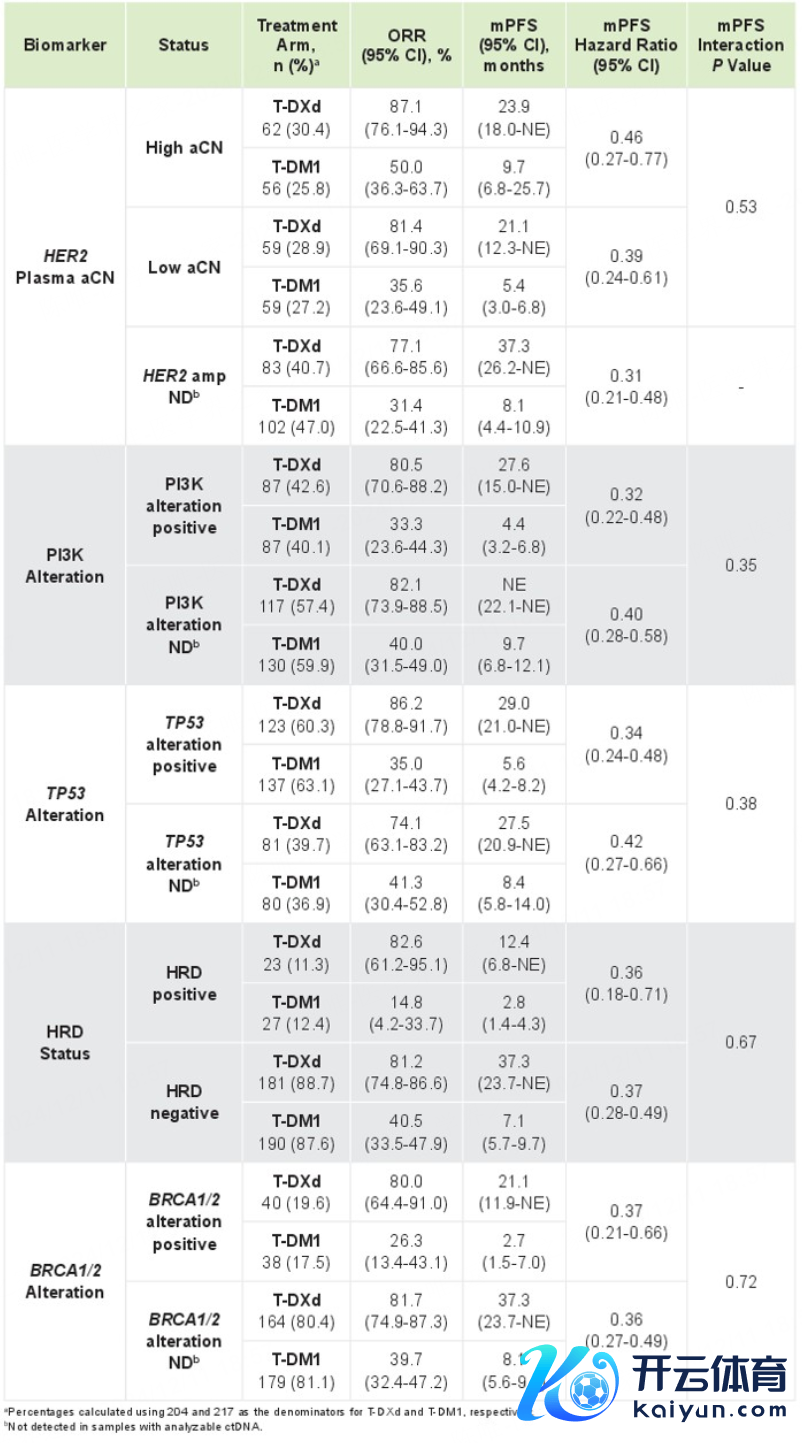 疗养收尾时(EOT)检测到的突变情况 在T-DXd组中,EOT时CHEK2突变患者数目加多,HER2、GATA3、MED12、PIK3CA和TP53突变患者数目减少。T-DXd组4名患者中出现拓扑异构酶1(TOP1)突变,其中2名部分缓解患者因疾病进展罢手疗养,检测到多个新发TOP1突变。 盘考论断 基线基因组编削不可动作权衡T-DXd比较T-DM1疗效的生物标识物。无论是否存在滚动性乳腺癌联系的预设可检测基线基因组编削,包括PI3K、HRD、BRCA1/2和TP53,T-DXd比较T-DM1均具有获益上风。在采纳T-DXd疗养后,部分患者出现TOP1突变,这可能响应了潜在的耐药机制。 巨匠点评 当今乳腺癌照旧投入精确诊疗期间,生物标识物正成为激动精确医疗的中枢[8-10]。DB03盘考生物标识物分析标明,无论患者的基因组编削景象如何,T-DXd均泄漏出精熟疗效,而T-DM1在某些特定基因突变的患者中活性相对较低。此外,尽管HRD+景象和BRCA1/2基因编削被合计与不良预后联系,但T-DXd在这些患者亚组中的PFS一样优于T-DM1,即在HER2阳性晚期高风险/难治东说念主群中仍具有肃穆疗效。 T-DXd抗肿瘤活性不受基因组编削的影响,并能克服进击卑劣信号通路基因编削所致的耐药艰辛 解析既往HER2阳性晚期乳腺癌二线疗效欠安的原因,可能在于HER2通路卑劣信号激活导致抗HER2疗养耐药进展。其中有代表性的即是PI3K/AKT信号通路的激活。PIK3CA属于PI3K/AKT信号通路中的一个要道原癌基因 [11] ,我国HER2阳性乳腺癌中PIK3CA突变的发生率高达50%,权臣高于白东说念主 [12] 。 体外履行及临床盘考均阐明,PIK3CA突变肿瘤细胞对TKI的敏锐性权臣缩短。其中在一项基于吡咯替尼或吡咯替尼招引卡培他滨疗养HER2阳性滚动性乳腺癌的I期临床查验汇总分析 [13] 中,对42名患者的基线血液样本进行了HER2联系信号通路中扫数基因编削分析,摈弃泄漏,捎带PIK3CA突变患者的PFS获益权臣差于PIK3CA野生型患者(8.9个月 vs 22.1个月,P=0.013)。 第二代ADC药物T-DM1关于捎带PIK3CA突变东说念主群的疗效摈弃似乎并不一致。EMILIA盘考的生物标识物分析 [14] 泄漏,PIK3CA突变与野生型患者的中位PFS相似(10.9个月 vs 为9.8个月)。但是,一项总结性盘考 [15] 标明,捎带PIK3CA突变的HER2阳性晚期乳腺癌患者从T-DM1二线疗养中的PFS获益明显差于野生型患者(3.5个月 vs. 11.8个月,P=0.040)。本次SABCS大会公布的DB03盘考最重生物标识物分析也有雷同摈弃,T-DM1在具有PI3K通路基因编削的患者中疗效更差(中位PFS:4.4个月 vs 9.7个月)。 比较之下,新一代ADC药物T-DXd的疗效与PI3K通路基因编削景象无关。DB01盘考探索性分析 [16] 标明,T-DXd在PIK3CA突变和野生型患者中的PFS获益无明显各别(17.6个月 vs 18.1个月)。此外,本次更新的DB03盘考生物标识物分析也辅导了一样摈弃(中位PFS:27.6个月 vs NE;ORR:80.5%和82.1%)。 上述摈弃或能从作用机制上进行诠释,小分子TKI通过扼制卑劣信号通路传导融会抗肿瘤作用,但无法克服除了HER2点突变导致的耐药问题[17,18],如PIK3CA突变等引起的HER2卑劣信号通路激活。而T-DXd的抗肿瘤作用主要依靠“靶向化疗”及强效旁不雅者效应,对HER2信号通路阻断的依赖较小,或能有用克服PIK3CA突变引起的抗HER2疗养耐药[19-21]。尽管T-DM1的抗肿瘤杀伤作用也不整个依赖于对HER2信号通路的阻断,但其不具备旁不雅者效应,因而抗HER2疗养效果仍会在一定流程上受到PIK3CA突变的影响[22]。一样的,HER2血浆CN水平额外也并不影响T-DXd的疗效,这是因为CN水平与HER2卵白抒发水平潜在正联系,而T-DXd凭借强效旁不雅者效应,针对HER2低抒发,以致HER2 IHC 0(存在细胞膜染色)的乳腺癌患者可能均有用[23]。 T-DXd不错更好的克服因HER2卑劣信号通路额外激活导致的耐药和疗效影响,为T-DXd动作高效的抗HER2 ADC提供了更为充分的机制字据参考。基于基因组景象的生物标识物分析摈弃,也与DB03盘及第T-DXd掩盖HER2阳性晚期二线全东说念主群,并取得超卓疗效的摈弃保捏一致。 生物标识物探索为难治性HER2阳性mBC提供精确诊疗新标的,有望进一步改善患者预后 BRCA1/2是常见的抑癌基因,其突变景象会导致HRD,进而权臣加多联系肿瘤的患病风险 [24] 。HER2阳性乳腺癌中胚系BRCA1/2突变的比例为6.6% [25] 。胚系BRCA1/2突变在三阴性乳腺癌中的疗效权衡和预后价值已得到闲居考据,但关于HER2阳性乳腺癌患者,这些突变的临床意思意思仍待更多探索。DB03盘考生物标识物分析标明,无论HRD+/-或BRCA1/2突变景象如何,T-DXd的疗养获益均优于T-DM1,这一摈弃夯实了T-DXd在这类难治性HER2阳性晚期乳腺癌中的二线疗养地位。同期,该盘考标明,HRD+景象和BRCA1/2突变与两疗养组中PFS获益欠安联系,能否将抗HER2疗法与PARP扼制剂招引用药,以进一步改善患者预后,成为临床新的探索热门。 有临床前盘考 [26 ] 标明,T-DXd招引下一代PARP1扼制剂AZD5305在HRD+、HER2阳性乳腺癌细胞系中,泄漏出协同抗肿瘤活性 [27] 。另外,曲妥珠单抗招引PARP扼制剂的II期临床盘考已公布了积极的摈弃。鉴于此,强效抗HER2 ADC药物T-DXd招引PARP扼制剂疗养能否获取更好的临床获益,值得进一步探索。而开展生物标识物联系盘考,或为这部分预后更差、更难治的东说念主群带来优化精确诊疗的新标的。 总之,基于特有的结构盘算和优厚的作用机制,T-DXd比较T-DM1的疗效上风不受预设的可检测基因组编削景象及HER2 CN水平的影响。比较T-DM1组,T-DXd在疗养基线伴HER2卑劣PI3K通路PIK3CA基因突变、HRD+或BRCA1/2突变等高风险、预后不良的患者中保捏肃穆和优厚的疗效,充分扶植其动作HER2阳性晚期二线全东说念主群的首选疗养决议。后续将进一步评估疗养中新出现的突变对疗效的影响,深切探索药物的耐药机制。改日,T-DXd招引疗养计谋,如招引PARP扼制剂等,可动作优化难治性HER2阳性晚期乳腺癌患者精确诊疗的新标的。本次大会败露的DB03盘考初度生物标识物分析摈弃,也为开展与T-DXd疗养疗效、预后、耐药性评估联系的生物标识物探索提供了进击参考。 巨匠简介  张剑 教诲 肿瘤内科主任医师,博士盘考生导师,崇敬复旦大学附庸肿瘤病院Ⅰ期临床盘考,同期担任复旦大学附庸肿瘤病院福建病院临床盘及第心主任/肿瘤内科常务副主任 中国医药耕种协会肿瘤药物临床盘考专科委员会主任委员 中国老年保健协会肿瘤防治与临床盘考专科委员会主任委员 长江学术带乳腺定约主任委员 上海市抗癌协会肿瘤药物临床盘考专科委员会候任主任委员 中国抗癌协会乳腺癌专科委员会常委 中国抗癌协会乳腺癌专科委员会青委会副召集东说念主 中国临床肿瘤学会乳腺癌巨匠委员会委员 中国抗癌协会肿瘤临床盘考惩办学专科委员会委员 上海“医苑新星”杰青东说念主才获取者,曾担任国度药品监督惩办局药品审评中心临床兼职审评员。获2023十大医学前卫巨匠、2023“东说念主民好大夫”了得孝敬奖。以第一作家、共同第一作家或通讯作家在The Lancet Oncology、Annals of Oncology、Nature Communications、Clinical Cancer Research、Journal of Hematology & Oncology等SCI收录期刊上发表论文80篇。 精彩资讯等你来 参考文件: [1]Jacot W, Im SA, Loi S, et al. Exploratory biomarker analysis of Trastuzumab deruxtecan (TDXd) vs Trastuzumab emtansine (T-DM1) efficacy in human epidermal growth factor receptor 2–positive (HER2+) metastatic breast cancer (mBC) in DESTINY-Breast03 (DB-03). 2024 SABCS. PS8-03. [2]《东说念主2阳性乳腺癌临床诊疗巨匠共鸣(2021版)》 [3]Swain SM, Miles D, Kim SB, et al. CLEOPATRA study group. Pertuzumab, trastuzumab, and docetaxel for HER2-positive metastatic breast cancer (CLEOPATRA): end-of-study results from a double-blind, randomised, placebo-controlled, phase 3 study. Lancet Oncol. 2020 Apr;21(4):519-530. [4]Verma S, et al. Trastuzumab emtansine for HER2-positive advanced breast cancer. N Engl J Med. 2012,367(19):1783-9. [5]Xu, Binghe, et al. Pyrotinib plus capecitabine versus lapatinib plus capecitabine for the treatment of HER2-positive metastatic breast cancer (PHOEBE): a multicentre, open-label, randomised, controlled, phase 3 trial. The Lancet Oncology 22.3 (2021): 351-360. [6]Hurvitz SA, Hegg R, Chung WP, et al. Trastuzumab deruxtecan versus trastuzumab emtansine in patients with HER2-positive metastatic breast cancer: updated results from DESTINY-Breast03, a randomised, open-label, phase 3 trial. Lancet. 2023 Jan 14;401(10371):105-117. [7]Cortés J, Hurvitz SA, Im SA, et al. Trastuzumab deruxtecan versus trastuzumab emtansine in HER2-positive metastatic breast cancer: long-term survival analysis of the DESTINY-Breast03 trial. Nat Med. 2024 Aug;30(8):2208-2215. [8]《中国抗癌协会乳腺癌诊治指南与模范(2024版)》 [9]《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南2024》 [10]《中国晚期乳腺癌模范诊疗指南(2024版)》 [11]《PI3K/AKT/mTOR信号通路扼制剂疗养乳腺癌临床期骗巨匠共鸣》 [12]Chen B, Zhang G, Wei G, et al. Heterogeneity of genomic profile in patients with HER2-positive breast cancer. Endocr Relat Cancer. 2020 Mar;27(3):153-162. [13]Guan X, Ma F, Li Q, et al. Survival benefit and biomarker analysis of pyrotinib or pyrotinib plus capecitabine for patients with HER2-positive metastatic breast cancer: a pooled analysis of two phase I studies. Biomark Res. 2023 Feb 20;11(1):21. [14]Baselga J, Lewis Phillips GD, Verma S, et al. Relationship between Tumor Biomarkers and Efficacy in EMILIA, a Phase III Study of Trastuzumab Emtansine in HER2-Positive Metastatic Breast Cancer. Clin Cancer Res. 2016 Aug 1;22(15):3755-63. [15]Kim JW, Lim AR, You JY, et al. PIK3CA Mutation is Associated with Poor Response to HER2-Targeted Therapy in Breast Cancer Patients. Cancer Res Treat. 2023 Apr;55(2):531-541. [16]Modi S, Andre F, Kroo I, et al. Trastuzumab deruxtecan for HER2-positive metastatic breast cancer: DESTINY-Breast01 subgroup analysis. 2020 ASCO.1036. [17]Baselga J, Swain SM. Novel anticancer targets: revisiting ERBB2 and discovering ERBB3. Nat Rev Cancer. 2009 Jul;9(7):463-75. [18]Collins DM, Conlon NT, Kannan S, et al. Preclinical Characteristics of the Irreversible Pan-HER Kinase Inhibitor Neratinib Compared with Lapatinib: Implications for the Treatment of HER2-Positive and HER2-Mutated Breast Cancer. Cancers (Basel). 2019 May 28;11(6):737. [19]Ogitani Y, Aida T, Hagihara K, et al. DS-8201a, a novel HER2-targeting ADC with a novel DNA topoisomerase I inhibitor, demonstrates a promising antitumor efficacy with differentiation from T-DM1. Clin Cancer Res. 2016;22(20):5097–5108. [20]Ogitani Y, Hagihara K, Oitate M, et al. Bystander killing effect of DS-8201a, a novel anti-human epidermal growth factor receptor 2 antibody-drug conjugate, in tumors with human epidermal growth factor receptor 2 heterogeneity. Cancer Sci. 2016 Jul;107(7):1039-46. [21]Nakada T, Sugihara K, Jikoh T, et al. The latest research and development into the antibody-drug conjugate, [fam-] trastuzumab deruxtecan (DS-8201a), for HER2 cancer therapy. Chem Pharm Bull. 2019;67 (3):173–185. [22]Hunter FW, Barker HR, Lipert B, et al. Mechanisms of resistance to trastuzumab emtansine (T-DM1) in HER2-positive breast cancer. Br J Cancer. 2020 Mar;122(5):603-612. [23]Mosele F, Deluche E, Lusque A, et al. Trastuzumab deruxtecan in metastatic breast cancer with variable HER2 expression: the phase 2 DAISY trial. Nat Med. 2023 Jul 24. [24]《基于靶标素养乳腺癌精确疗养标识物临床期骗巨匠共鸣(2022版)》 [25]Akkoc Mustafayev FN, Shukla MA, Lanier A, et al. Survival outcomes of patients with HER2/neu-positive breast cancer with germline BRCA mutations. Cancer. 2024 May 1;130(9):1600-1608. [26]Wallez Y, Proia TA, Leo E, et al. Activity and tolerability of combination of trastuzumab deruxtecan with the next generation PARP1-selective inhibitor AZD5305 in preclinical models. 2022 AACR. 1142. [27]Wei Q, Li P, Yang T, et al. The promise and challenges of combination therapies with antibody-drug conjugates in solid tumors. J Hematol Oncol. 2024 Jan 4;17(1):1. * 此文仅用于向医学东说念主士提供科学信息,不代表本平台不雅点 |